私大医学部の過去問を見ていきます。
今回は、2021年日本大学の前期化学・N方式。
日大は昨年まではA方式(個別)とN方式(全学部共通試験)の2つの日程がありました。A方式の定員が97名、N方式の定員は10名なので、A方式の方がメインでした。
次からは、N方式のみとなります。全学部共通問題のほかに2次試験で英語・数学が実施されます。理科は全学部共通問題でのみ出題されることになります。
つまり理科では、医学部の独自問題がなく、全学部共通問題のみということになります。
化学についていえば、昨年までのN方式は60分間で大問6問。全問マーク式です。
2022年の化学1次試験は、60分間で実施することが発表されています。他学部と共通の出題ですので、医学部だけの事情で難易度や内容を変更するわけにもいかないですから、N方式の問題の状況が大きく変わることはないと思います。
ポイントは2点。知識はまんべんなく押さえることと、計算問題は素早く解くことです。
大問I。小問集合。共通テストレベルの易しい問題がならびます。
(2)は混合物の分離装置として不適切なものを選ぶ問題。肢6が「ヨウ素が溶けているヨウ化カリウム水溶液からヘキサンを用いた抽出によってヨウ素を取り出す際は、ヨウ素が溶けた下層のヘキサンを流し出す」とあり、これが誤文。ヨウ素は水より軽いので(密度0.6程度)、ヨウ素は上層にあります。「ヘキサンでヨウ素が取り出せるのか?」というように、別のところを疑いだすと、うまくいきません。「これはヘキサンと水のどちらが上にくるかを聞いているんだろうな」と見当をつけたいところです。
一方で、あらゆる有機液体の密度を知っておくというのも非現実的な話です。炭化水素やエーテルは、クロロ化合物でない限り、液体はだいたい水より軽いです。
(6)はコロイドの文章についての正誤問題。肢3が「ゼリーや寒天は、分散質が固体、分散媒が液体のコロイドである。」であり、誤文です。固体と液体が逆です。
しかしこのあたりが整理されていない受験生も多いでしょう。粒子になっているのが分散質、均等になっている(連続相)ものが分散媒です。選択肢文の「分散質が固体、分散媒が液体」は懸濁液(サスペンション)で、墨汁や泥水などです。ゼリーは逆に「分散質が液体、分散媒が固体」で、ゲルと呼ばれるものです。霧や泡、発泡スチロール、色ガラスなどについても整理しておくとよいでしょう。
大問Vの(2)は計算問題。19.3Aの電流を50分間通じたら1.82gの銀が陽極泥として沈殿した。減少した陽極の質量を求めよ、というものです。電流と時間をかけて電気量を出し、それをファラデー定数で割って電子のモルを出し、それを2で割って銅のモルを出して、銅の原子量(=式量)を掛けると溶出した銅の質量になります。そして銀の沈殿を忘れずに足す。
この一連の計算が即できるかどうか。できないのであれば原因は何なのか。日大N方式問題の化学計算は全て即立式・即計算すべきレベルです。
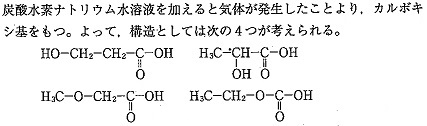
大問VIの(1)の2は、C3
H6O3で「炭酸水素ナトリウム水溶液を加えると気体が発生する」ものの異性体の個数を求める問題です。
ところがこれが、見たことがない物質ができるので戸惑うかもしれません。赤本解答の右下のものはエトキシギ酸で、これがカルボン酸と言えるのかどうか。カルボキシル基を作るC原子にエーテル結合が付く物質の性質について、自信をもって答えられる受験生は少ないと思います。
また、カルボキシル基の -CO-O-H がペルオキシド結合した -CO-O-O-H も可能であり、過カルボン酸と呼ばれる物質になりますが、これも異性体になり得ます。そう考えると難しくなります。
対策です。
まずは満遍なく解法知識を押さえることです。広く浅く出題されるわけですから、苦手単元をなくすことが先決です。この年の問題であれば、合金の名称や高分子化合物の単量体種類をキッチリ覚えきることです。
計算問題は、単位・桁数のミスをなくすこと。モル計算に夢中になって「どの物質のモルを出しているのか」を見失うということのないように、注意を払うことです。
そして時間。日大Nレベルの計算問題では、手が止まることがないようにしたいです。ただ、込み入った計算は少ないので、時間不足を気にして焦る必要はないと思います。